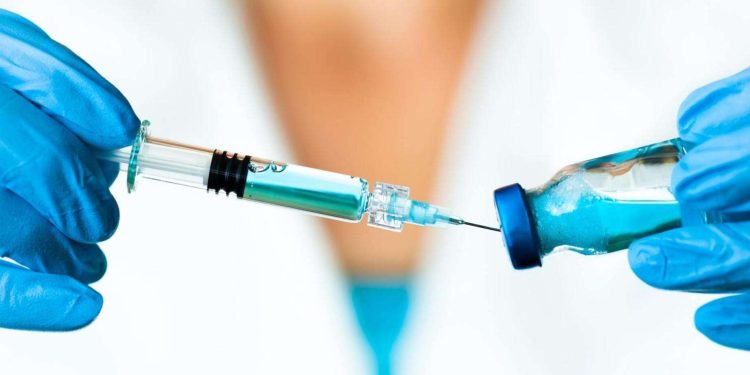
- La vacuna Patria, desarrollada por el Laboratorio Avimex, recibió autorización de emergencia. por parte de la Cofepris
- La aprobación se basó en un riguroso análisis técnico y evaluación clínica.
- Cofepris destaca que sus autorizaciones son reconocidas por más de 20 países en América Latina y el Caribe.

La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) ha otorgado la autorización para uso de emergencia a la vacuna Patria, desarrollada por el Laboratorio Avimex S.A. de C.V., contra el Covid-19.
Análisis y aprobación de Cofepris
Esta autorización resulta de un riguroso análisis técnico y de la evaluación del desempeño clínico de la vacuna, llevado a cabo en la sesión del Comité de Moléculas Nuevas (CMN) el pasado 26 de enero. La sesión fue pública y la resolución fue unánimemente favorable.
“El equipo multidisciplinario de dictamen confirmó que la vacuna mexicana Patria cumple los más altos estándares de calidad, seguridad y eficacia, conforme a los datos presentados en el expediente técnico ante esta comisión y permite su uso en las instituciones públicas que conforman el sector Salud”, afirmó Cofepris.
Continuidad y reconocimiento internacional
De acuerdo con el Decreto que declara el fin de la emergencia sanitaria por Covid-19, las autorizaciones emitidas por Cofepris que se encuentren vigentes conservarán su validez mientras los medicamentos e insumos sean necesarios para la continuidad de la Política Nacional de Vacunación contra el SARS-CoV-2 y el plan de gestión a largo plazo de la Secretaría de Salud.
Más de 20 países en América Latina y el Caribe reconocen las autorizaciones de Cofepris, lo que facilita el acceso a esta vacuna sin necesidad de nuevas evaluaciones. Este reconocimiento internacional subraya la rigurosidad y la experiencia de Cofepris como agencia reguladora de nivel 4, comparable con la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y la Agencia Europea de Medicamentos (EMA).